Сегодня в Воронеже стремительно развивается радиотерапевтическая служба. Научно-клинический онкологический центр в достаточной мере обеспечен оборудованием для проведения лучевой терапии на самом современном уровне, где сконцентрированы высоко квалифицированные кадры радиотерапевтов и медицинских физиков, используются высоко технологичные методики предлучевой топометрической подготовки и лучевого лечения.
Термин «брахитерапия» берет свое начало от греческого слова др.-греч. βραχύς, что в переводе означает «короткий». На заре прошлого столетия в 1908г. — впервые применяется методика внутриполостного облучения с применением радия для лечения рака матки. В 1910 году американские ученые Д. Пасто и П. Дегрэ разработали методику лечения, обеспечивавшую доставку необходимой дозы радиоактивного вещества к пораженному органу, не прибегая к тотальному облучению организма пациента. С тех пор было разработано несколько основных систем, включая Парижскую, Стокгольмскую и Манчестерскую, на основе внутриполостной лучевой терапии с использованием радиоактивного источника радия. С 1938 года стала использоваться манчестерская система «точки А», которая определялась с помощью рентгеновской визуализации, но не учитывала индивидуальную анатомию или видение опухоли. Отсутствие объемной визуализации приводила в ряде случаев к недостаточному охвату опухоли при брахитерапии, а также в выраженной токсичности на здоровые окружающие органы. Чтобы избежать нехватки системы «точки А», Комиссия по радиационным единицам и измерениям (ICRU) в отчете 38 в 1985 году предложила концепцию целевого объема и определены референтные точки для мочевого пузыря и прямой кишки.
Исторически внутриполостная лучевая терапия в Воронежском онкоцентре стала применяться в 60-х гг. прошлого века, когда использовалось ручное введение источников Co60 низкой мощности излучения, которое было сопряжено с высокой лучевой нагрузкой на медицинский персонал. Для введения в полость матки использовались линейные источники Co60 активной длиной 6 см, заключенные в цилиндры или препараты активной длиной 1 см. Источники вводились в резиновом катетере, число которых определялось в зависимости от длины полости матки и цервикального канала, во влагалище вводились препараты длиной 1см (рис.1).
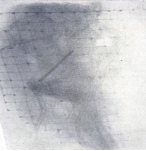
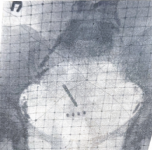
Рис.1 Рентгенограмма малого таза с введенными источниками Co60
И в последующем развитие данного метода получило в двух этапном последовательном введении аппликаторов в полость матки и затем уже радиактивных источников с целью улучшений радиактивной безопасности для персонала. Были разработаны специальные устройства для этих целей – аппликаторы (рис 2,3). В полость вводятся эндостаты (линейной, объемной или шаровидной формы), а затем в них вручную вводился Co60 в герметизированной оболочке. Суммарная активность источников излучения 70мг экв. радия. Продолжительность сеанса составляла 24-48 часов, №3-4.

Рис. 2 Аппликатор для внутриполостной лучевой терапии.
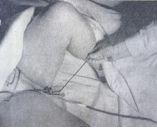
Рис.3 Введение радиактивных источников
Автоматизированная контактная лучевая терапия стала использоваться в радиогинекологическом отделении с 1997г, когда был поставлен отечественный гамма-терапевтический аппарат «Агат –ВУ» с источником излучения Co60 высокой мощности дозы, позволяющий проводить планирование по рентгеновским снимках (рис 4, 5). При внутриполостном введении широко распространен метод афтерлоадинга (от англ. afterloading – последующая нагрузка). Облучение проводилось на шланговом аппарате «АгатВУ». Этот метод стал применяться во всем мире, вытеснив ручное введение источников. Недостатком на тот момент был расчет на плоскости (2Д) с использованием унифицированных шаблонов. Основное ограничение заключалось в том, что расчет основывался на аппликаторе и точке, и, следовательно, отсутствовала пространственная информация об объемах опухоли и объемах критических органов.

Рис. 4 Отечественный шланговый аппарат «Агат-ВУ»

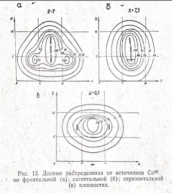
Рис.5. Планирование по рентгеновским снимках на точку А при раке шейки матки.
После 1990-х годов значительные технологические достижения привели к использованию методов визуализации для сбора трехмерных данных, внедрению инструментальных средств оконтуривания как объемов мишени, так и объемов критических органов, новых алгоритмов планирования и оптимизированного по объему планирования лечения для применений как дистанционной лучевой терапии, так и брахитерапии, наряду с новыми конструкциями аппликаторов и аппаратов для афтерлодинга при брахитерапии. И в 2007г отделение было переоснащено современным гамма-терапевтическими аппаратами «GammaMedplus iX» с источником иридий 192, с 3-D планирующими программами, BrachyVision 14.0, Vitesse 2.5. Оснащение данным аппаратом позволило в дальнейшем специалистам Воронежского онкологического диспансера перейти на планирование с использованием изображений компьютерной или магнттно-резонансной томографии при планировании контактной лучевой терапии. В 2012г заведующая отделением Коротких Н.В. прошла обучение по брахитерапии рака предстательной железы в университетской клинике «Шлезвиг-Гольштейн» город Киль, Германия. Врачи БУЗ ВО ВОНКОц первыми стали проводить данный метод среди онкологических клиник Центрального Черноземья. В настоящее время проводится внутритканевая лучевая терапия при раннем раке молочной железы, саркомах мягких тканей, орофаренгиальных опухолей. В связи с возрастающей потребностью в контактной лучевой терапии в 2020г был приобретен еще один аппарат «Gamma Med plus iX» с источником иридий 192, производства фирмы с 3-D планирующими программами, BrachyVision 16.0, Vitesse 3.0 (рис. 6), что позволило проводить брахитерапию рака пищевода.

Рис. 6. аппарат «GammaMedplus iX» с источником иридий 192.
На сегодняшний день в радиотерапевтическом отделении №5 БУЗ ВО ВОНКОЦ выстроена вся технологическая цепочка, позволяющая проводить 3Д планирование контактной лучевой терапии с использование изображений, получаемых не только с использованием компьютерной (16-срезовых томографах с широкой апертурой, используемые для подготовки больных к лучевой терапии), но и магнитно-резонансной томографии. Магнитно-резонансный томограф Philips Ingenia 1.5T MR-RT для поддержки и планирования лучевой терапии, имеет преимущества для минимизации неточностей при планировании.
Расчет планов лучевого лечения осуществляется на сложнейших системах планирования (Vitesse, BrachyVision). Использование современных планирующих программ позволяет составлять оптимальные планы лечения, распределять равномерно дозы излучения, которые охватывают весь объем опухоли, не затрагивая здоровые органы и ткани (рис.7).
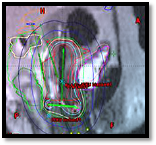
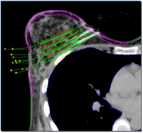
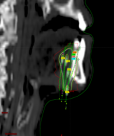
Рис. 7. Планирующая компьютерная программа BrachyVision

Дозы на органы риска, получаемые пациентом во время процедуры лечения, контролируются с помощью in vivo дозиметрии. Система фиксирует ошибки, связанные с отказом оборудования, в доставке дозы, позиционирования аппликатора и изменениями анатомии пациента.
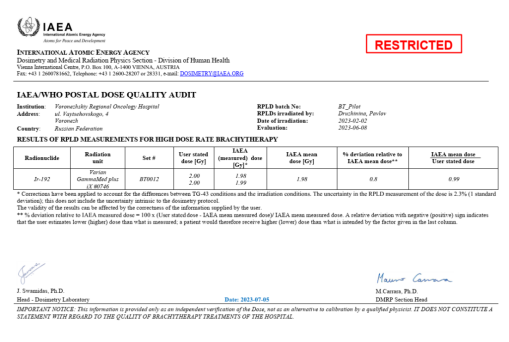
Радиотерапевтическая служба БУЗ ВО ВОНКОЦ успешно прошла дозиметрический аудит в Лаборатории МАГАТЭ, Австрия, поучен сертификат качества. МАГАТЭ признала проведение брахитерапии в Воронежском областном научно-клиническом центре на высоком уровне.
Брахитерапия значительно изменилась из эпохи 2-D в эпоху 3-D и, причем это огромное развитие обусловлено значительными технологическими достижениями за последние годы. Современная брахитерапия – ценный современный и комплексный инструмент в лечении злокачественных опухолей. Специалисты в области брахитерапии во всем мире возлагают большие надежды на применение технологии 3D-печати индивидуальных аппликаторов для обеспечения персонализированного лечения с потенциалом улучшения показателей выживаемости. Современные достижения 3D-печати позволяют создавать персонализированный аппликатор индивидуальной конструкции, соответственно анатомии пациента достигая оптимальной точности распределения дозы.
Мы с оптимизмом смотрим в будущее! Дальнейшее развитие брахитерапии открывает новые горизонты в лечении онкологических пациентов.

